comitéProfesionales
Entradas para Profesionales
¿Puede ser preventiva la inmunoterapia con alergenos inhalantes en niños?
Las enfermedades alérgicas suponen una carga de salud que afecta a todos los grupos de edad y que pueden manifestarse temprano en la vida como dermatitis atópica, alergia alimentaria, rinitis/conjuntivitis alérgica y asma alérgica.
En una revisión bibliográfica recientemente publicada por Dwived y col.1 revisan las estrategias de prevención que se pueden implementar en cada etapa de la vida:
- Primaria: se dirige a niños, preferiblemente recién nacidos, que están en alto riesgo de desarrollar enfermedades alérgicas pero que aún no están sensibilizados. El objetivo en esta etapa es prevenir el desarrollo de sensibilizaciones y el consiguiente inicio de una enfermedad alérgica.
- Secundaria: involucra a niños sensibilizados antes de la aparición de síntomas. Este enfoque se centra en la prevención de nuevas sensibilizaciones y el inicio de nuevas enfermedades alérgicas.
- Terciaria: se dirige a niños con enfermedades alérgicas existentes. Los objetivos en esta etapa son prevenir la progresión de la enfermedad alérgica existente a otra y prevenir nuevas sensibilizaciones.
Dado que el sistema inmunológico es más plástico en la primera infancia, esta etapa se considera ideal para llevar a cabo medidas para prevenir enfermedades alérgicas. En este sentido, se han investigado los efectos preventivos de la inmunoterapia con alérgenos (AIT). La evidencia para aplicar la inmunoterapia preventiva con alérgenos (pAIT) está creciendo rápidamente, aunque aún enfrenta desafíos debido a factores relacionados con la edad y que los datos son limitados.
Esta revisión presenta un resumen actualizado de la evidencia disponible sobre aspectos preventivos de AIT con alérgenos respiratorios en nuevas sensibilizaciones, inicio y progresión de enfermedades alérgicas, así como otros efectos inmunomoduladores, centrándose particularmente en niños.
Los autores realizaron una búsqueda en PubMed, Embase y el Registro Central de Ensayos Controlados de Cochrane (CCRCT) para estudios pediátricos sobre AIT con alérgenos inhalantes. Se evaluaron 33 publicaciones de 27 cohortes. En estos informes, participaron 2952 niños y 1491 fueron tratados activamente.
Según los datos obtenidos, la prevención primaria con pAIT parece segura, aunque con resultados inciertos. En uno de los ensayos se observó una efecto preventivo para nuevas sensibilizaciones transitorio y no alérgeno-específico al final del tratamiento (pero no durante ni tras el tratamiento). La reducción en la proporción de asma solo se evidenció después de una prolongación en uno de los estudios. Por tanto, este enfoque plantea algunos retos que aclarar, incluyendo la identificación de sujetos y la optimización de la dosis y duración efectivas.
La prevención secundaria sí demostró ser viable y segura según esta revisión. En un ensayo clínico doble ciego controlado con placebo se evaluó la prevención secundaria en niños asintomáticos y sensibilizados a ácaros o polen de gramíneas. Tras dos años de tratamiento con inmunoterapia sublingual, en este estudio no se observó una prevención en nuevas sensibilizaciones y tampoco mostró datos en relación al inicio de la enfermedad alérgica. Sin embargo, se describieron efectos pro-tolerogénicos como el desarrollo de IgG específica en el grupo activo y la inducción de citoquinas reguladores: Il10 y TGF-b. Por tanto, los niños en edad preescolar sensibilizados pero asintomáticos podrían ser objeto de intervención a este nivel de prevención.
La prevención terciaria fue estudiada en 28 publicaciones. Cambios en la tasa de sensibilización fueron reportados en 13 grupos al final del tratamiento. 6 de ellos observaron protección frente a nuevas sensibilizaciones en los grupos activos. En 9 publicaciones se evidenció un efecto tras el tratamiento en desarrollo de nuevas sensibilizaciones. 4 de ellos reportaron efectos favorables, mientras que en uno se observó un incremento en nuevas sensibilizaciones en el grupo activo. En 3 de 5 cohortes hubo un efecto de la pAIT sobre la progresión de la rinoconjuntivitis alérgica. La persistencia a largo plazo de este efecto se observó en 2 cohortes. 5 estudios que analizaban parámetros inmunomoduladores reportaron efectos favorables al final y tras el tratamiento (incremento en los niveles de IgG e IgG4 específicas, citoquinas reguladoras o niveles bajos de eosinófilos). Por tanto, a nivel de prevención terciaria, los resultados sobre la eficacia de la pAIT en nuevas sensibilizaciones o la progresión de la enfermedad alérgica se describen de manera inconsistente. Los autores concluyen que evaluar la eficacia de este enfoque es complejo y requiere más ensayos, particularmente enfocados en aspectos preventivos.
Los posibles mecanismos subyacentes a la inducción de tolerancia en AIT se han observado en niveles de prevención terciaria y secundaria, pero no en el nivel primario. Para la prevención primaria, algunos autores sugirieron que la inducción de tolerancia específica de alérgeno podría requerir un paso obligatorio que implicara la activación transitoria de la inmunidad primaria. En los otros niveles de prevención (secundaria y terciaria), los posibles mecanismos tolerogénicos incluyen la regulación positiva de IgG1 e IgG 4, principalmente, pero también IgA1 e IgA2. Estos anticuerpos pueden poseer capacidad neutralizante y podrían competir con IgE por el alérgeno. También pueden prevenir la activación de mastocitos y basófilos e inducir células B, que secretan estos anticuerpos bloqueadores y son responsables de la inmunotolerancia a largo plazo. Otras respuestas celulares implican la reducción del reclutamiento de eosinófilos, la supresión de células Th2 y la inducción de poblaciones de células reguladoras (de células linfoides innatas, células dendríticas, células T y B) y respuestas de citoquinas reguladoras (IL10 y TGF β), restableciendo el equilibrio Th1-Th2.
Según los autores, los efectos diferenciales de pAIT en cada etapa del desarrollo de niños y adolescentes deben ser evaluados para identificar la ventana de oportunidad para la prevención. Enfatizan en un inicio temprano de pAIT, ya que tener como objetivo el sistema inmunológico infantil puede ofrecer beneficios preventivos más efectivos y duraderos. Tener una sensibilización, especialmente polisensibilizaciones, a la edad escolar ya eleva el riesgo de asma en la edad adulta. Por lo tanto, los niños entre 5 meses y la edad preescolar, con un riesgo alto de desarrollar alergias debido a antecedentes familiares positivos, teniendo un menor grado de sensibilización y sin síntomas alérgicos o con síntomas leves, parecerían óptimos para pAIT.
El pAIT de ácaros es el más comúnmente estudiado. A diferencia de las mezclas heterogéneas de alérgenos, la aplicación de monoterapia de ácaros para la prevención primaria mostró un efecto protector sobre el desarrollo de nuevas sensibilizaciones.
Se ha establecido que la administración de AIT debe durar 2–3 años para lograr una inmunotolerancia duradera. Se están explorando regímenes de tratamiento más cortos, aunque el valor definitivo de los mismos aún no se ha aclarado, particularmente para enfoques de prevención primaria y secundaria.
Los autores de la revisión concluyen explicando que la eficacia global de pAIT sigue sin aclararse en niños debido a la naturaleza multifactorial de los resultados. La prevención secundaria parece factible y puede inducir inmunotolerancia. La prevención terciaria usando pAIT de pólenes de gramíneas y/o árboles parece ser capaz de prevenir la progresión de rinoconjuntivitis a asma, aunque los beneficios de pAIT basada en otras fuentes de alérgenos no son concluyentes. Es necesario definir la dosis óptima de alérgenos, adyuvantes y vías de administración.
La infancia representa una ventana de oportunidad para iniciar medidas profilácticas, pero se necesitan ensayos pediátricos adicionales bien diseñados para comprender los efectos preventivos de la AIT sobre las nuevas sensibilizaciones, el inicio y la progresión de enfermedades alérgicas junto con los beneficios inmunomoduladores.
Mercedes Ramírez Hernández. Complejo Hospitalario Universitario de Cartagena.Comité de Alergia Infantil SEAIC.
Bibliografía:
1,. Varsha Dwived, Sonja Kopanja, Klara Schmidthaler, Justyna Sieber, Christina Bannert, Zsolt Szépfalusi. Preventive allergen immunotherapy with inhalant allergens in Children. Allergy. 2024;79:2065–2087. DOI: 10.1111/all.16115
Captador de la semana: Cáceres

En el captador de la semana hoy os traemos al Dr. Sergio Porcel Carreño, alergólogo que realiza su labor asistencial en el Hospital Universitario de Cáceres, desde donde nos proporciona los datos para la red aerobiológica de la SEAIC.

Recordamos que podéis consultar los recuentos de pólenes en vuestra ciudad en www.polenes.com
¿Si he tenido una reacción con Amoxicilina, qué antibióticos podría utilizar hasta ser valorado por alergología?
La amoxicilina es uno de los antibióticos más utilizados para el tratamiento de infecciones respiratorias, urinarias, dentales, de la piel, etc. También se utilizan para prevenir infecciones, o antes de algunos procedimientos diagnósticos o intervenciones quirúrgicas.
Pertenece a la familia de los antibióticos betalactámicos, y a este grupo pertenece también la penicilina, que es el antibiótico más antiguo conocido, así como otros muchos antibióticos pertenecientes a diferentes subfamilias como cefalosporinas, carbapenems o monobactams.
Cualquier antibiótico puede producir diferentes tipos de reacciones adversas, algunas conocidas y relacionadas con la dosis del antibiótico, por ejemplo, dolor abdominal, deposiciones diarreicas o infecciones por hongos en mucosa oral o genital. Tras este tipo de reacciones, y según la intensidad de la sintomatología, puede ser necesario suspender el tratamiento. Hay otro tipo de reacciones no predecibles, como son las reacciones alérgicas o de hipersensibilidad, que pueden aparecer incluso a dosis mínimas, y pueden ser desde muy leves a graves.
Cuando un paciente en tratamiento con amoxicilina presenta síntomas no relacionados con la infección que está tratando, debe consultar en un centro sanitario. Si los síntomas que presenta son efectos secundarios conocidos, será su médico el que valore la continuación de ese antibiótico, o el cambio a uno de la misma familia o de otra familia, según la infección que esté tratando. En estos casos se podría seguir tomando antibióticos de la familia de los betalactámicos.
Cuando su médico considere que presenta síntomas sugestivos de una reacción alérgica a la amoxicilina siempre debe ser valorado y estudiado en una Unidad de Alergología, y hasta entonces no debe tomar ningún antibiótico de la familia de los antibióticos betalactámicos. Hoy en día existen múltiples alternativas como antibióticos del grupo quinolonas, macrólidos, lincosamidas, aminoglucósidos, tetraciclinas y sulfamidas entre otros.
Es muy importante que este tipo de reacciones sean estudiadas ya que la sospecha de ser alérgico a antibióticos betalactámicos implica la evitación de un gran número de fármacos que son muy utilizados en la actualidad, y tras el estudio nos podrán dar alternativas dentro de este mismo grupo terapéutico.
María Salas Cassinello
Hospital Regional Universitario de Málaga
Captador de la semana: Badajoz
Hoy os presentamos al Dr. Jesús García Menaya, médico alergólogo que realiza su labor asistencial en el Hospital Universitario de Badajoz, desde donde nos aporta los recuentos de pólenes. El Hospital de Badajoz tiene un largo recorrido con los contajes de pólenes ya que llevan realizándolo desde los años 80, inicialmente por el Dr. Indalecio González Galán y desde el 2003 por el Dr. Jesús García.
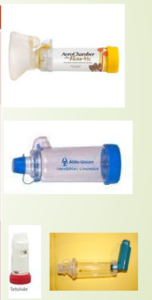
CÁMARAS DE INHALACIÓN
No son dispositivos de inhalación propiamente dichos, pero su utilización está ampliamente recomendada para evitar problemas relacionados con la técnica de los inhaladores de cartucho presurizado. Es un espaciador que separa la boquilla del cartucho presurizado de la boca del paciente. Por este motivo antiguamente se denominaban a estos aparatos “espaciadores” y hoy en día se utilizan ambos nombres de manera indistinta (cámaras de inhalación o cámaras espaciadoras)
Poseen una válvula en su boquilla habitualmente unidireccional que permite la inspiración del aire de la cámara, pero no la espiración dentro de ella.
Su uso enlentece la velocidad de salida del aerosol y evapora el propelente. Las partículas de aerosol pequeñas se mantienen unos segundos en suspensión en espera de ser inhaladas, y las grandes chocan con las paredes de la cámara y quedan retenidas. De esta forma se produce un menor depósito orofaríngeo y se aumenta el depósito pulmonar. El uso de la cámara inhalatoria permite utilizar menor cantidad de fármaco, reduciendo los efectos secundarios, tanto sistémicos como locales y, por eso, se aconseja en caso de disfonía debida al uso de los inhaladores. Además, eliminan la dificultad de coordinar la inspiración con la pulsación del dispositivo.
Se utilizan en el tratamiento de las exacerbaciones de asma (excepto las de riesgo vital), ya que el efecto broncodilatador administrado con cámara de inhalación es equivalente al de un nebulizador y es una alternativa en pacientes con bajo flujo inspiratorio.
Al igual que con los diferentes inhaladores es importante adiestrar al paciente en el uso de la cámara inhalatoria y revisar la técnica periódicamente.
Tipos de cámaras
Existen cámaras de diferentes tamaños desde 140-800 ml. Son universales, permitiendo su conexión a los diferentes modelos de inhaladores de cartucho presurizado, son portátiles y se pueden utilizar con mascarillas faciales. 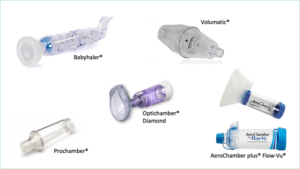
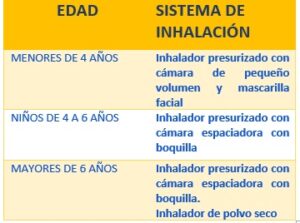
Recomendaciones de uso de dispositivos de inhalación según edad
Elaboración propia (Modificado de GEMA- Inhaladores,2018)
Limpieza y mantenimiento de las cámaras
- Son de uso personal
- Limpiar semanalmente, si se usa a diario, con agua templada y detergente suave o neutro, separando las piezas y por inmersión.
- Dejar secar las piezas al aire, sin frotar para no aumentar la carga electrostática que contribuye a que las partículas del aerosol se peguen en las paredes de la cámara.
- Hay que reemplazarlas cuando tengan fisuras.
Ventajas e inconvenientes
Errores en el uso de la cámara inhalatoria
-No agitar el inhalador de cartucho presurizado
-No adaptar bien el inhalador a la cámara.
-No adaptar bien la cámara al rostro o no usar la cámara adecuada a la edad del paciente.
-No realizar un adecuado mantenimiento y limpieza cámara
-No enjuagar la boca
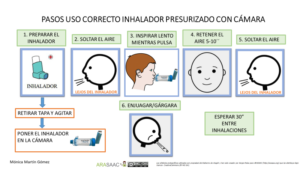
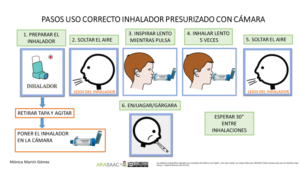
Técnica de uso de la cámara inhalatoria
1- Destapar el inhalador y agitarlo
2- Mantener el inhalador en vertical con la boquilla en la parte inferior.
3-Vaciar los pulmones lentamente, hasta donde sea cómodo
4- Colocar la boquilla, entre los labios y los dientes, evitando que la lengua obstruya la salida de la boquilla. Comenzar a inhalar lentamente, a través de la boca y al mismo tiempo presionar el dispositivo para activar una dosis. (también se puede presionar primero y a continuación inhalar lenta y profundamente)
5-Mantener una inhalación lenta y profunda, a través de la boca, hasta que los pulmones estén llenos de aire.
6-Aguantar la respiración entre 5 y 10 segundos y soplar lentamente (En caso de agudización se puede inhalar y exhalar en cinco ocasiones sin retirar la cámara de la boca y también en menores de 5 años)
7-Cerrar el dispositivo de inhalación
8- Hacer gárgaras y enjuagar la boca al terminar
Imagen 1.- Técnica de uso de cámara de inhalación con presurizado (adultos y niños > 5 años)
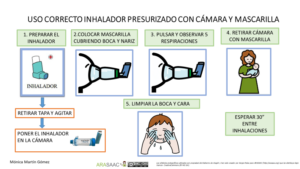
Imagen 2.- Técnica de uso de cámara de inhalación con presurizados niños < 5años
Imagen 3.- Técnica de uso de cámara de inhalación con presurizado en lactantes
En el caso de los lactantes y menores de 5 años que no sepan realizar apnea, se usa una cámara de inhalación con mascarilla del tamaño adecuado para que se adapte a la cara del niño/a.
1.-Se prepara el inhalador previamente: se agita, se retira la tapa y se conecta a la cámara.
2.-Se pulsa solo 1 vez mientras se mantiene la mascarilla en la cara del niño/a cubriendo boca y nariz.
3.-Debe respirar al menos 5 veces (observaremos la válvula de la cámara).
4.-Esperar 30 segundos para nueva inhalación si precisa.
5.- Limpiar la cara y boca del niño/a.
BIBLIOGRAFÍA
- Romero de Ávila G, Gonzálvez Rey J, Mascarós Balaguer E. AGAMFEC. Las 4 reglas de la terapia inhalada [Internet]. Disponible en: https://www.agamfec.com/wp/wp-content/uploads/2015/05/Las4reglasdelaterapiainhalada.pdf
- Plaza V Giner J, Bustamente V, Viejo A, Flor X, Maiz M, et al. GEMA inhaladores. Terapia inhalada: fundamentos, dispositivos y aplicaciones prácticas [internet]. Luzan 5, editor. Madrid; 2018.Disponible en: www.gemasma.com
- Giner J, Plaza V, López-Viña A, Rodrigo G, Neffen H, Casan, P. Consenso SEPAR-ALAT sobre terapia inhalada [internet]. Arch Bronconeumol. 49. 2-14; 2013. Disponible en: http://www.archbronconeumol.org/ el 09/07/2013.
- Gema 5.4. Guía española para el manejo del asma [Internet]. Madrid: Ed. Luzán5; 2024. Disponible en: http://.www.gemasma.com.
- Gema educadores. Manual del educador en asma [Internet]. Madrid: Ed. Luzán5; 2010. Disponible en: http://.www.gemasma.com.
LA ATOPIA COMO PRIMERA MANIFESTACIÓN DE ERROR INNATO DE LA INMUNIDAD
Es importante iniciar por definir que es un error innato de la inmunidad (EII) siendo un grupo de enfermedades causadas por defectos genéticos que generan disfunción inmunitaria. 1
La alergia como manifestación inicial de EII se reporta con una media de hasta el 8 % de los pacientes con diagnostico de errores innatos de la inmunidad variando entre 5 al 25 % y se ha observado un retraso en el diagnóstico de hasta 6 a 10 años, las característica que comparte estos pacientes suele ser la triada típica de la alergia presentado eosinofilia+ igE elevada + Eccemas, por ende estos paciente suele debutar con diagnósticos en un mayor porcentaje de dermatitis atópica en un 21.38% asociadose principalmente inmunodeficiencias combinadas como síndrome de hiper Ig-E (HIES), la deficiencia de DOCK 8, el síndrome de Omenn (OS) y el síndrome de Wiskott-Aldrich (WAS). Sin embargo, otros estudios reportan una mayor asocia con alergia a nivel de vías respiratorias relacionándose con el asma bronquial hasta el 46.90%, en cuanto a rinitis alérgica su frecuencia fue de 8.2 %, presentándose una mayor asociación en paciente con deficiencias en anticuerpos, y en especial con inmunodeficiencia selectiva de IgA. Las alergias alimentarias se presentaron en menor prevalencia (0.10%) y se asocia con inmunodeficiencia selectiva de IgA. 2
A nivel fisiopatológica se ha observado que en los pacientes con función normal de sistema inmune, las infecciones activan los linfocitos Th1 y Th2, estas infecciones también favorecen al desarrollo de los linfocitos Tregs, que ayudan mantener el equilibrio entre los Th1 y Th2, y prevenir sus efectos nocivos, en el caso de los pacientes con errores innatos de la inmunidad se observa que las linfocitos Tregs pueden estar ausentes o deficientes a nivel funcional, desencadenando una mayor activación de Th1 y Th2 y por ende una susceptibilidad mayor a desarrollar alergias o cuadros de autoinmunidad.
La asociación entre alergia y error innato de la inmunidad puede representar una alteración del equilibrio complejo dentro del sistema inmunológico de células efectoras y reguladoras, quizás también contribuida por diferencias en la colonización microbiana y patrones de infección, muy probablemente debido a falla de tolerancia, defectos de señalización del receptor de células T, falla de producción de interferón-gamma contrarregulador y exceso de producción de citocinas como IL-13 que interfieren con los péptidos antimicrobianos de la piel , así como alteración de la barrera cutánea. 3
- El aumento de la permeabilidad de la piel por el eccema lleva a que las células presentadoras de antígenos (CPA) cutáneas se expongan a mayores cantidades de antígenos ambientales habitualmente inocuos. Esto conduce a la sensibilización y la producción de citocinas proinflamatorias asociadas a Th2, lo que inicia en consecuencia la respuesta alérgica 4,5. La alteración de la barrera cutánea junto con la regulación negativa de los péptidos antimicrobianos protectores aumenta el riesgo de infección 5.
- Las citocinas proinflamatorias de tipo 2 también regulan negativamente la filagrina, una proteína importante para la integridad de la barrera cutánea, lo que aumenta la permeabilidad de la piel, permitiendo una mayor exposición a los antígenos y por ende una mayor respuesta inflamatoria 4,5
Los defectos a nivel de barrera cutánea y el desarrollo de dermatitis atópica en estos pacientes se relación con alteraciones en la barrera, defectos genéticos como la producción de filagrina, spink 5, anomalías del citoesqueleto; señalización aberrante del TCR; señalización interrumpida de citocinas; disminución de la diversidad del repertorio de células T y trastornos del desarrollo tímico; mecanismos efectores de células innatas; y trastornos metabólicos.
Es importante tener en cuenta que los pacientes con deficiencia selectiva de IgA pueden desarrollar un gran espectro de enfermedades desde ser asintomáticos a debutar con infecciones recurrente, enfermedades de autoinmunidad y enfermedades alérgicas hasta en el 13- 84%, en el caso de la patología alérgicas estas sueles ir disminuyendo con la edad. 6
Existen características con las cuales podemos sospechar de una probable asociación con errores innatos de la inmunidad :
- Biomarcadores elevados de TH2 (eosinofilia: 1500, IgE elevado: >2000 en los 3 primeros meses)
- Antecedentes familiares: Consanguinidad, antecedentes muertes tempranas familia.
- Cutáneo: disposición de eccemas en regiones poco frecuentes de neonatos, eritrodermia, ictositosis al nacimiento, alteraciones a nivel de dentición, alteraciones a nivel de tejido conectivo (hiperlaxitud). DOCK8: Eccemas severos predominantemente a nivel de zona de flexuras, facial, zona del pañal, liquenificaciones, infecciones virales.
- Hematológico: Pancitopenia, anemia hemolítica, purpura
- Infecciosos: Infecciones severas y recurrentes especialmente por CMV, EBV, HHV6 y patógenos de la familia Herspesviridae, candidiasis mucocutánea, eccema herpeticum.
- Gastroenterológico: falla de medro, diarreas y vómitos persistente
- Endocrinopatías: Diabetes tipo I, Tiroiditis autoinmune.
- Respiratorio: presencia de bronquiectasias, mala respuesta a tratamiento.
Sin embargo es importante tener en consideración que los niveles de IgE no siempre se correlacionan con cuadros de errores innatos de inmunidad, por lo que se debe descartar otras patologías que puedan elevar tanto IgE como eosinófilos entre estas tenemos diferentes causas como:
INFECCIOSAS
- Parásitos: Helmintos como Toxocaria, Strongyloides, Trichuris, Áscaris.
- Bacterias: Mycobacterium Tuberculosis
- Virales: CMV, VEB, VIH
ONCOLÓGICAS
- Gammapatías o síndromes paraneoplásicos
- Linfoma cutáneo de células T
- Enfermedad de Sézary
- Linfoma de Hodking y no Hodking
ENFERMEDADES INFLAMATORIAS
- Granulomatosis eosinofílica con poli angeítis (EGPA)
BIBLIOGRAFIA
1.Tangye, S.G.; Al-Herz, W.; Bousfiha, A.; Cunningham-Rundles, C.; Franco, J.L.; Holland, S.M.; Klein, C.; Morio, T.; Oksenhendler, E.; Picard, C.; et al. Human Inborn Errors of Immunity: 2022 Update on the Classification from the International Union of Immunological Societies Expert Committee. J. Clin. Immunol. 2022, 42, 1473–1507. [CrossRef] [PubMed]
- El-Sayed et al. World Allergy Organization Journal (2022) 15:100657 http://doi.org/10.1016/j.waojou.2022.100657
3.Sokol, K.; Milner, J.D. The overlap between allergy and immunodeficiency. Curr. Opin. Pediatr. 2018, 30, 848–854. [CrossRef] [PubMed]
4.Facheris, P.; Jeffery, J.; Del Duca, E.; Guttman-Yassky, E. The translational revolution in atopic dermatitis: The paradigm shift from pathogenesis to treatment. Cell. Mol. Immunol. 2023, 20, 448–474. [CrossRef] [PubMed]
- Lyons JJ, Milner JD. Primary atopic disorders. J Exp Med 2018; 215:1009–1022. 6. & Nelson RW, Geha RS, McDonald DR. Inborn errors of the immune system associated with atopy. Front Immunol 2022; 13:860821. This article provides a comprehensive overview of atopy in relation to IEIs.
- Boyarchuk, o. (2018). Allergic manifestations of primary immunodeficiency diseases and its . Asian journal of pharmaceutical and clinical research, 1-8.
Importancia de la correcta identificación del niño con anafilaxia en Urgencias pediátricas
La mayoría de las guías nacionales e internacionales de anafilaxia recomiendan a nuestros pacientes acudir a urgencias después de un episodio de anafilaxia, independientemente de que se hayan tratado o no.
La puerta de entrada de todos ellos en Urgencias es el triaje. Allí, el personal, habitualmente de enfermería, decidirá en pocos minutos, cuándo, quién y donde serán atendidos. En esto consiste la priorización o triaje.
Todos sabemos que la anafilaxia es una reacción de hipersensibilidad potencialmente mortal y que por ello requiere el máximo nivel de prioridad. Sin embargo, los pocos datos disponibles muestran que estos pacientes no se identifican correctamente, reciben una prioridad menor que la merecen y reciben tratamiento tarde, con riesgo de empeorar su pronóstico.
Hasta la fecha, los datos disponibles acerca de la priorización del paciente con anafilaxia se han limitado a hospitales seleccionados y a sistemas de triaje específicos.
Desde el Comité de Alergia Infantil de Seaic, nuestro objetivo ha sido conocer y describir la priorización que reciben los niños con anafilaxia en España. Este es el primer estudio que revisa la priorización de la anafilaxia pediátrica más allá de un solo centro, superando las barreras de los múltiples sistemas de triaje existentes en España. Los participantes en el estudio trabajan en 36 hospitales de 12 comunidades autónomas distintas. Su conocimiento acerca de que anafilaxia es una emergencia que merece atención médica inmediata es correcto. Sin embargo, su aplicación práctica no lo es al analizar la prioridad que recibirían casos reales. Asi, los niños con anafilaxia probablemente son identificados de forma incorrecta en los servicios de urgencias pediátricas en España, lo que puede empeorar su pronóstico.
La anafilaxia debería identificarse en triaje para garantizar un tratamiento precoz y adecuado.
Los alergólogos podemos ayudar a mejorar el triaje del niño con anafilaxia por nuestro conocimiento acerca de sus peculiaridades, variedades en la presentación clínica, ausencia de datos patognomónicos, y porque aportamos un punto de vista que complementa la visión del especialista en Urgencias.
“Anaphylaxis must be suspected in triage. Triage advice regarding anaphylaxis identification should be included in anaphylaxis guidelines”
J Investig Allergol Clin Immunol 2025; Vol. 35(4)(enlace a la versión del artículo) doi10.18176_jiaci.1064.pdf
Esozia Arroabarren Aleman. Servicio de Alergología del Hospital Universitario de Navarra. Comité de Alergia Infantil de la Sociedad Española de Alergia e Inmunología Clínica
NOVEDADES
La necesidad de información y educación del paciente con patología alérgica, es una
necesidad constante que aparece reflejada en todas las guías clínicas. En este sentido
la figura de las enfermeras de los servicios de alergia es fundamental para que los
pacientes adquieran conocimientos y desarrollen habilidades para mejorar tanto su
calidad de vida como el control de su enfermedad.
Un ejemplo en este sentido, de divulgación y educación, es la entrevista que realizaron
a nuestra compañera Silvia Castro Fernández del Hospital Abente y Lago de A Coruña
en el medio digital Mundiario.
Enlace al artículo:
PREVISIONES PÓLENES 2025
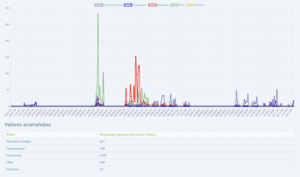
El pasado jueves 20 de marzo tuvo lugar la rueda de prensa en la que el Dr. Juan José Zapata, presidente del comité de Aerobiología Clínica, dio a conocer las previsiones de pólenes para esta primavera.
El año 2024 ha sido extremadamente cálido, y en cuanto a la hidrología ha sido un año normal o ligeramente húmedo para la mayor parte de la península. En general se espera una primavera intensa, a continuación compartimos un resumen de las previsiones de gramíneas por zonas. Añadir que se han cumplido las previsiones para la primavera del 2024.
LAS PREVISIONES, DE UN VISTAZO
ISLAS CANARIAS
Primavera muy leve.
200- 250 granos/m 3 (Tenerife, Las Palmas)
CORNISA CANTÁBRICA, NAVARRA, LA RIOJA y GALICIA
Primavera leve: 1500-2000 gr/m3, (Bilbao, San Sebastián, La Coruña, Lugo, Pontevedra,
Orense, Santander, Oviedo)
Primavera moderada:
3.200 granos/m3 (Logroño)
4.800 granos/m3 (Pamplona)
Primavera intensa:
5.200 gr/m3 (Vitoria)
LITORAL MEDITERRÁNEO
Primavera leve: Baleares, Cataluña, Comunidad Valenciana y Murcia
CENTRO PENINSULAR
Primavera leve: Aragón.
Primavera moderada-intensa: Castilla-León, Castilla- La Mancha y Madrid.
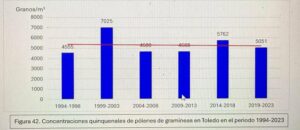
Primavera intensa: Toledo (6.000 granos/m 3 ).
SUR PENINSULAR
Primavera leve: Almería, Cádiz, Málaga y Huelva.
Primavera moderada: Córdoba y Granada.
Primavera intensa: Badajoz, Cáceres, Sevilla y Jaén.
16.000-19.000 granos/m 3 (Cáceres y Badajoz).
Puede consultar los datos actuales de pólenes en su ciudad en la web www.polenes.com
CARAT: una herramienta validada para evaluar el control del asma y la rinitis alérgica en la práctica clínica
El Control of Allergic Rhinitis and Asthma Test (CARAT) es un cuestionario diseñado para evaluar el control simultáneo del asma y la rinitis alérgica (RA) en los pacientes, mediante una evaluación retrospectiva de cuatro semanas. Recientemente, un estudio ha realizado una revisión sistemática y un meta-análisis siguiendo las directrices de COSMIN, con el objetivo de evaluar sus propiedades psicométricas.
¿Por qué usar CARAT en la práctica clínica?
La evaluación del control del asma y la rinitis alérgica suele realizarse por separado, con herramientas como el Asthma Control Test (ACT) o el Allergic Rhinitis Control Test (ARCT). Sin embargo, dado que la mayoría de los pacientes con asma también padecen rinitis alérgica, surge la necesidad de una herramienta unificada. CARAT cubre esta brecha con 10 preguntas sobre síntomas de vías respiratorias superiores e inferiores, calidad del sueño, impacto en la actividad diaria y uso de medicación.
Propiedades psicométricas de CARAT
En esta revisión sistemática se incluyeron 16 estudios con los que se concluye que CARAT posee:
- Buena validez de contenido y una adecuada estructura factorial.
- Alta consistencia interna (α de Cronbach = 0.83).
- Alta fiabilidad (coeficiente de correlación intraclase = 0.91).
- Buena validez de constructo, con correlaciones significativas con otros PROMs (ej. ACT y ACQ-5).
- Buena capacidad de respuesta (cambio mínimo importante de 3.5 puntos).
Aplicación práctica
CARAT puede ser administrado en consulta mediante papel puesto que está validado al idioma castellano, pero también está disponible en formato digital a través de aplicaciones móviles como MASK-air y plataformas web, permitiendo un monitoreo continuo del paciente.
Conclusión
Esta revisión sistemática y meta-análisis refuerzan el uso de CARAT como una herramienta confiable para el control del asma y la rinitis alérgica en la práctica clínica habitual. Su implementación puede mejorar el seguimiento de los pacientes y facilitar decisiones terapéuticas más precisas
BIBLIOGRAFIA
Vieira RJ, Sousa-Pinto B, Cardoso-Fernandes A, et al. Control of Allergic Rhinitis and Asthma Test: A systematic review of measurement properties and COSMIN analysis. Clin Transl Allergy. 2022;12(9):e12194.
Diana Q, Abraham A, Yaicith A, Peter O, Juan T. Validation of the Spanish language version of the control of allergic rhinitis and asthma test. NPJ Prim Care Respir Med. 2022;32(1):47. Published 2022 Oct 29.
Sousa-Pinto B, Sá-Sousa A, Amaral R, et al. Assessment of the Control of Allergic Rhinitis and Asthma Test (CARAT) using MASK-air. J Allergy Clin Immunol Pract. 2022;10(1):343-345.e2.
CLASIFICACIÓN DE LA IT SEGÚN SU FORMULACIÓN LA IMPORTANCIA DE LOS EXTRACTOS
La Organización Mundial de la Salud (OMS) define la Inmunoterapia (IT) con alergenos como el único tratamiento que puede alterar el curso natural de la patología alérgica y prevenir el desarrollo del asma en pacientes con rinitis alérgica. Es el único tratamiento dirigido a la causa de la patología, a diferencia de los tratamientos de los síntomas, siendo fundamental que los extractos de las vacunas sean de alta calidad para que sean efectivas.1
Es importante cuando administremos dichos tratamientos tener una noción básica de los tipos de vacunas específicas de alergia. Con este documento tratamos de mostrar una clasificación breve de los tipos de IT especifica de alergia que en este momento se utilizan en su uso clínico en los servicios de alergología de nuestro país.
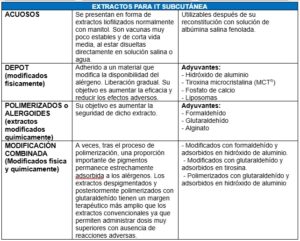
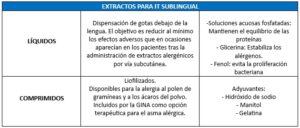
Los extractos para inmunoterapia subcutánea (ITSC) pueden ser acuosos, depot, polimerizados o modificación combinada. En la inmunoterapia sublingual (ITSL) la composición del extracto alergénico es la misma que en la ITSC, pero se modifica el excipiente. Los excipientes pueden ser líquidos o comprimidos liofilizados.
Se debe seguir las indicaciones realizadas por los laboratorios fabricantes en su forma de administración y las posibles modificaciones de la pauta que realice el clínico en atención a las características específicas de cada paciente.
Bibliografía:
- Abramson M, Puy R and Weiner J Inmunotherapy in Asthma; an update systematic review. Allergy 1999,54, 1022-1041.
Captador de la semana: Oviedo
Desde el Hospital Central de Asturias, la doctora Dolores Quiñones, alergóloga, realiza los contajes con el nuevo captador de la red de la SEAIC instalado en 2024.
Los datos de todas las estaciones aerobiológicas de la SEAIC pueden consultarse en la web www.pólenes.com
Reuniones Comité Aerobiología
A continuación se adjuntan las últimas dos reuniones del comité celebradas en Santiago de Compostela en octubre del 2023 y en Bilbao en noviembre 2024.
Reintroducción de la leche de vaca en bebés con alergia IgE mediada utilizando la Escalera de la Leche
¿Qué es la Escalera de la Leche?
La Escalera de la Leche es una intervención estructurada diseñada para ayudar a los bebés con alergia a la leche de vaca a reintroducirla gradualmente en su alimentación. Se inicia con alimentos que contienen pequeñas cantidades de leche bien cocida y avanza hasta productos con un mayor contenido de leche. Este enfoque progresivo busca progresar en la dieta. Desarrollada en el Reino Unido, ha sido ampliamente utilizada en alergia no IgE-mediada pero nuestro grupo ha estudiado su aplicabilidad, seguridad y eficacia en alergia a la leche IgE-mediada en lactantes recién diagnosticados de alergia a la leche.
Adaptación de la Escalera de la Leche para familias españolas:
La Escalera de la Leche original fue desarrollada por dietistas en el Reino Unido e incluye alimentos que comúnmente se consumen en ese país. Dado que los hábitos alimentarios varían según la cultura, nuestro primer objetivo fue desarrollar una versión de la Escalera de la Leche adaptada a la dieta tradicional española con recetas específicas. La versión española de la Escalera de la Leche consta de cuatro niveles, en los que se introducen alimentos con cantidades crecientes de leche de vaca y esta está progresivamente menos cocinada. El nivel inicial consiste en galletas, pan de leche y magdalenas y se progresivamente se introducen alimentos como tortitas, croquetas o bechamel. Por último, se introduce el yogurt y la leche.
Información relevante y resultados del estudio:
Este estudio se llevó a cabo de 3 hospitales de Madrid e incluyó bebés de menos de 1 año recién diagnosticados de APLV. Al cumplir los 12 meses, aquellos que seguían siendo alérgicos comenzaron la Escalera de la Leche. Los padres recibieron instrucciones y recetas para preparar los alimentos de cada nivel de la escalera. Se confirmó la tolerancia a cada nivel de la Escalera en el hospital mediante una provocación oral. Aquellos bebés que toleraban se les indicaba tomar a diario los alimentos de cada nivel y volver al cabo de 3 meses para continuar progresando en la Escalera. El 63.6% de los bebes no tuvo ninguna reacción y progresaron a lo largo de la escalera hasta conseguir reintroducir la leche y lácteos en la dieta. La mayoría de las reacciones ocurrieron en el hospital y aquellas que ocurrieron en casa fueron más leves y bien manejadas por los padres. La Escalera de la Leche fue una intervención segura para la mayoría de los pacientes, pero no está exenta de reacciones (algunas graves) por lo que requiere un control estricto por un Alergólogo.
La información completa está publicada en el artículo: Safety, Tolerability, and Feasibility of the Milk Ladder for Reintroduction of Cow’s Milk in Infants With IgE-Mediated Cow’s Milk Allergy. J Investig Allergol Clin Immunol. 2024 Dec 3;34(6):414-416.
Inmaculada Cerecedo
Allergy and Clinical Immunology Department, Cleveland Clinic Abu Dhabi, Emiratos Árabes Unidos
Sonsoles Infante
Unidad de Alergia Pediátrica, Servicio de Alergología, Hospital General Universitario Gregorio Marañón, Madrid
Belen de la Hoz
Servicio de Alergología, Hospital Universitario Ramon y Cajal, Madrid
Captador de la semana: Toledo
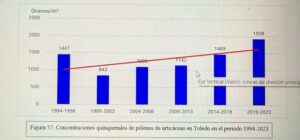
Hoy es el turno del Dr. Ángel Moral De Gregorio, expresidente del comité de Aerobiología Clínica de SEAIC, alergólogo en el Hospital Universitario de Toledo, desde donde nos proporciona los datos de pólenes.
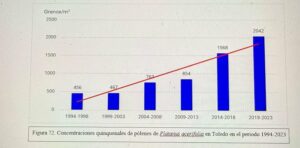
Se instaló el primer captador en 1994, en 2016 se instaló el ciclón, han resistido todas las inclemencias incluido Filomena en 2021.
Con el Curso Avanzado de Palinología, el Dr. Ángel Moral ha impartido cursos de palinología a más de 200 alergólogos, muchos de los cuales han continuado la labor de aportar la lectura de pólenes en su zona para pólenes.com SEAIC.
Además, el Dr. Ángel Moral así como el Hospital de Toledo han contribuido ampliamente al estudio de los pólenes a lo largo de los años.

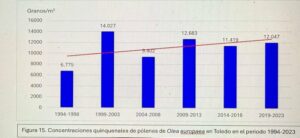
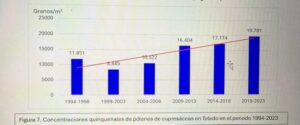

Dificultades diagnóstica en alergia a picadura de himenópteros
El diagnóstico de alergia a veneno de himenópteros consiste en identificar el veneno (o los venenos) responsable de causar reacción alérgica tras una picadura. Para este fin se cuentan con diversas técnicas diagnósticas como lo son las pruebas cutáneas, la determinación de IgE especifica, además de la información que proporciona el paciente sobre el insecto sospechoso.
Pero en ocasiones llegar a descubrir cual es el veneno responsable no es tan sencillo. Esto puede deberse a que: (1) el paciente no puede identificar el insecto que le ha picado, (2) las técnicas diagnósticas (pruebas cutáneas o la determinación de IgE especifica) son negativas, (3) presencia de resultados positivos a varios venenos y (4) discordancia entre el resultado de las pruebas cutáneas y los valores de IgE específica.
Para abordar estas dificultades es recomendable:
(1) Ampliar la historia clínica. Se debe de preguntar por la presencia de aguijón tras la picadura. Cuestionar si había alimentos cerca. Interrogar sobre el lugar donde sufrió la picadura (cerca de ríos, pantanos, lagos o piscinas). Recabar información sobre la presencia de colmenas próximas. Indagar sobre la visualización de nidos (terrestres o aéreos). Investigar sobre la profesión o “hobbies”. Es también muy importante conocer la región geográfica donde presentó la picadura.
(2) Optimizar las técnicas diagnósticas. Reducir el punto de cohorte de la IgE específica a 0,10 kU/L. Repetir las pruebas cutáneas o la determinación de IgE especifica pasados 1 a 2 meses. Ampliar el estudio a todos los venenos disponibles. Emplear otras técnicas diagnósticas más complejas.
(3) Diferenciar reactividad cruzada de doble sensibilización. Cuantificar alergenos especie específicos y alérgenos de reactividad cruzada. Establecer la ratio de antígeno 5 (en caso de resultados positivos para polistes y vespula). Identificar la presencia de CCD’s (en caso de resultados positivos para apis y vespula).
(4) Repetir estudio alergológico. Volver a realizar las pruebas cutáneas y determinación de IgE especifica. Valorar utilizar otro extracto diagnóstico al repetir las pruebas cutáneas. Aplicar plataformas multiplex.
Si tras haber completado todas las recomendaciones anteriores la identificación del veneno no es posible se puede intentar enviar suero del paciente a centros especializados que cuenten con la infraestructura y la experiencia para realizar técnicas diagnósticas más complejas (Test de activación de basófilos, Immunoblot o CAP-inhibición).
Lamentablemente enviar suero o derivar pacientes a otros centros no siempre es posible. A pesar de no poder establecer con una precisión del 100% el veneno (o los venenos) responsable de la reacción, el paciente subsidiario de beneficiarse de inmunoterapia específica para venenos debe recibirla. Si la reacción que presenta pone en riesgo su vida (anafilaxia) o implica un deterioro importante en su calidad de vida se le debe de administrar inmunoterapia específica contra todos los venenos identificados como probables responsables de la reacción.
Actualmente existen protocolos y guías clínicas que explican la forma en la que se debe de iniciar una doble inmunoterapia para veneno de himenópteros en aquellos pacientes que lo requieran. La administración de doble inmunoterapia es segura y confiere una buena protección en caso nuevas picaduras.
Federico de la Roca Pinzón
Médico Especialista en Alergología.
Miembro del comité de alergia a himenópteros.
TRATAMIENTO BIOLÓGICO EN LAS ENFERMEDADES ALÉRGICAS/ASMA GRAVE
Los medicamentos biológicos son producidos por organismos vivos o a partir de ellos (microorganismos humanos, animales o células de biotecnología) y se caracterizan por su alta especificidad y actividad terapéutica porque van dirigidos a la proteína o al receptor concreto que interviene en el proceso de la enfermedad.
Se consideran productos biológicos a las vacunas, alérgenos, antígenos, hormonas, inmunoglobulinas, citocinas, derivados de la sangre o plasma y anticuerpos monoclonales, entre otros.
Su auge se debe al gran avance de la biología molecular a través de técnicas de DNA recombinante, al conocimiento del genoma humano y de las vías de regulación de la respuesta inmune, que ha permitido identificar un variado número de dianas o puntos clave para este tipo de terapia.
El descubrimiento y producción de anticuerpos monoclonales (Ac Mo) por el Dr. Milstein en 1975 ha marcado la historia de la Medicina y Biotecnología. Inicialmente la indicación terapéutica se centró en áreas como reumatología y oncología, extendiéndose a diversas especialidades médicas como aparato digestivo, neurología, y también a la alergología.
La incorporación de anticuerpos monoclonales (Ac Mo) a la terapia alergológica ha significado un avance significativo en la medicina personalizada y de precisión, mejorando el manejo de las enfermedades alérgicas. Actúan bloqueando reguladores del sistema inmunitario claves en estas enfermedades.
Hasta el momento, en Alergología, los fármacos biológicos están indicados en:
- Asma Grave (Escalón 5-6 de la GEMA)
- Dermatitis Atópica
- Urticaria Crónica
- Esofagitis Eosinofílica, Síndrome Hipereosinofílico (SHE)
- Granulomatosis eosinofílica con poliangeítis (GEPA)
- Rinosinusitis Crónica con Poliposis Nasal (RSNCcPN)
- Angioedema Hereditario
Están en estudio algunos fármacos biológicos como tratamiento adyuvante en procesos de desensibilización con alimentos o medicamentos o inmunoterapia de alto riesgo, entre otros.
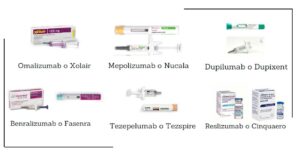 Imagen 1. Ejemplo de fármacos biológicos utilizados en alergología en la actualidad
Imagen 1. Ejemplo de fármacos biológicos utilizados en alergología en la actualidad
En general, el tratamiento biológico reduce los síntomas, disminuye el uso de glucocorticoides orales, así como los ingresos hospitalarios, lo que conlleva menos costes sanitarios. Además, mejora el control de la enfermedad y la calidad de vida del paciente.
La administración del fármaco se realiza en un centro sanitario (hospital o Centro de Salud) por enfermeras o bien se instruye y educa al paciente para que se pueda autoadministrar el fármaco en su domicilio, cuando la vía de administración es la subcutánea, ya que existen jeringas y plumas precargadas y preparadas para la inyección .
EFECTOS ADVERSOS MÁS HABITUALES
ADMINISTRACIÓN DOMICILIARIA
La enfermera, como educadora en autocuidados, es la encargada de evaluar si el perfil del paciente es adecuado para garantizar la seguridad de la administración, conservación, técnica adecuada y el cumplimiento del tratamiento en su domicilio.
Para ello, la enfermera, durante las primeras dosis administradas en el centro sanitario, educa y valora al paciente/cuidador en relación a los siguientes aspectos: Conservación, preparación, localización de la zona y la técnica correcta de inyección, efectos adversos y eliminación del residuo.
PRECAUCIONES A TENER EN CUENTA ANTES DE LA ADMINISTRACIÓN
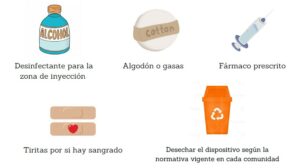
- Mantener el medicamento fuera de la vista y del alcance de los niños.
- No utilizar el medicamento después de la fecha de caducidad que aparece en el etiquetado.
- Conservar en nevera (entre 2-8º). No congelar ni calentar.
- Conservar en el embalaje original (esto lo protege de la luz).
- El envase que contiene el dispositivo precargado puede conservarse a temperatura ambiente (25º), antes de usarlo, de horas a días en función del biológico que tenga prescrito el paciente.
- No utilizar ningún envase que esté dañado o muestre indicios de deterioro.
- Visualizar el aspecto del fármaco antes de utilizarlo (que muestre un aspecto claro sin turbideces).
- No agitar el dispositivo precargado.
MATERIAL NECESARIO PARA LA AUTOADMINISTRACIÓN
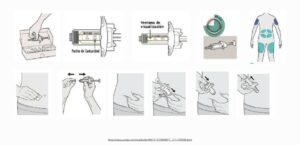
PASO A PASO AUTOADMINISTRACIÓN
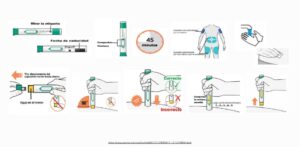
PLUMA PRECARGADA
JERINGA PRECARGADA
BIBLIOGRAFÍA
- Cuñetti L. Generalidades de los Medicamentos Biológicos [Internet]. Boletín farmacológico. 2014 [citado agosto 2024]. Disponible en: http://www.boletinfarmacologia.hc.edu.uy/index.php?option=com_content&task=view&id=104&Itemid=66
- Gema 5.4. Guía española para el manejo del asma. [Internet]. Madrid: Ed. Luzán 5; 2024. [citado agosto 2024]. Disponible en: http://.www.gemasma.com
- Iniciativa estratégica para el abordaje integral del asma: resumen ejecutivo. Disponible en : https://.seaic.org/profesionales/noticias-para-profesionales/libro-asma360.html (consultado julio 2024)
- Sabaté Brescó M, Salas Cassinello M, Sánchez Hernández MC, Sánchez Machín I, Sánchez Matas I, Sastre Domínguez J et al. El libro de las enfermedades alérgicas. [Internet]. Madrid: Fundación BBVA; 2021[citado agosto 2024]. Disponible en: https://www.fbbva.es/wp-content/uploads/2021/10/Libro-enfermedades-alergicas_FBBVA.pdf
- Delgado Romero J , Blanco-Aparicio M , Cisneros Serrano C , Díaz-Pérez D, Ferrando Piqueres R, López-Carrasco V, Merino-Bohórquez V , Soto-Retes L , Domínguez-Ortega J. Apoyo a la administración domiciliaria de terapia biológica en pacientes con asma grave: BioCart© [Internet].J Investig Allergol Clin Immunol 2022; Volumen 32(6): 482-484. Doi: 10.18176/jiaci.0786
- Ficha técnica autorizada de Xolair ® (omalizumab) (Consultado en septiembre 2024) Disponible en: https://cima.aemps.es/cima/dochtml/ft/05319008/FT_05319008.html
- Ficha técnica autorizada de Nucala® (mepolizumab) (Consultado en septiembre 2024)Disponible en: https://cima.aemps.es/cima/dochtml/ft/1151043001/FT_1151043001.html
- Ficha técnica autorizada de Fasenra ® (benralizumab) (Consultado en septiembre 2024)Disponible en : https://cima.aemps.es/cima/dochtml/p/1171252001/P_1171252001.html
- Ficha técnica autorizada de Dupixent® (dupilumab) (Consultado en septiembre 2024) Disponible en : https://cima.aemps.es/cima/dochtml/ft/1171229006/FT_117229006.html
- Ficha técnica autorizada de Tezspire® (tezepelumab) (Consultado en septiembre 2024) Disponible en: https://cima.aemps.es/cima/dochtml/ft/1221677001/FT_1221677001.html
Captador de la semana: Madrid – Clínica Subiza
Esta semana le toca el turno al Dr. Javier Subiza, primer Presidente del comité de Aerobiología Clínica, y Coordinador de la Red Nacional de Colectores de la Sociedad Española de Alergia (1993 – 2010). Creador de la primera página de la SEAIC de recuentos de pólenes. Actualmente desarrolla su actividad como alergólogo en la Clínica Subiza.


Historia de la estación de Aerobiología de Madrid (General Pardiñas 116).
En 1972, el Dr. Eliseo Subiza se desplazó a Londres al Hospital San Mary, el mismo en el que el Dr. Fleming descubrió la penicilina, para aprender la técnica que permitía hacer los recuentos de pólenes de una forma estandarizada, ese mismo año trae de allí el primer colector de pólenes volumétrico tipo Hirst que hubo en España.
En los siguientes años pudo publicar los primeros calendarios polínicos de Madrid y poco después del resto de España, gracias a que pudo instruir en esta técnica a muchos de sus colegas alergólogos(1,2).
El colector estuvo en la azotea de esta clínica desde 1973 hasta 1982, en que fue sustituido por otro colector tipo Hirst (Burkard 7 day recording volumetric spore trap). Del 2002 al 2012 fue expuesto en el museo de ciencias naturales de Valencia y desde entonces lo hemos recuperado de nuevo para exponerlo de forma permanente en nuestro centro (Clínica Subiza).
El Dr. Javier Subiza ha seguido los pasos de su padre, coordinando desde 1994 hasta el 2010, la red de colectores de la Sociedad Española de Alergología e Inmunología Clínica, creando en 1995 de forma pionera para visualizarse en Internet, la primera página oficial de recuentos de pólenes de la SEAIC (www.polenes.com). Otros logros, junto con su equipo, han sido descubrir por primera vez un método fiable que permite predecir en una gran parte de España los recuentos de pólenes de gramíneas con dos meses de antelación y que se sigue utilizando hasta la fecha (3).
Otros logros importantes han sido descubrir en la década de los 90, la capacidad alergénica de algunos pólenes de árboles, tales como los de Platanus hispanica y Cupresáceas, desconocidos hasta entonces, como causa importante de polinosis en España y que se han convertido en la actualidad, en una causa importante de polinosis de invierno e inicio de la primavera, en muchas de las áreas de nuestro país (4,5).
En 2021 dimos a conocer junto con nuestra colega la Dra Martha Cabrera la presencia de Phl p 1 clínicamente relevante, en periodos sin granos de pólenes atmosféricos, fuera de la estación de gramíneas (6).
Recientemente hemos podido dar a conocer como el cambio climático, ha producido en Madrid un incremento de 1,3° en los últimos 45 años. Ello parece haber contribuido a un adelanto de la estación y un incremento muy importante de los pólenes atmosféricos, especialmente los de invierno, lo que a su vez parece haber condicionado un aumento de la prevalencia de sensibilización, a Cupressus, Platanus y Quercus, este último coincidiendo con los hallazgos previamente encontrados por la Dra María Pedrosa (7,8).
Referencias
1) Subiza Martín E. Incidencia de granos de pólenes en la atmósfera de Madrid. Método volumétrico. Allergol et immunopatol. Supplementum VII, 1980.
2) Subiza E. Informe de 17 estaciones de España (método volumétrico). Incidencia de pólenes. En: XIV Congreso Nacional de la SEA. Madrid: Alergia e Inmunología Abelló, 1984; 41-43.
3) Subiza J, Masiello JM, Subiza JL, Jerez M, Hinojosa M, Subiza E. Prediction of annual variations in atmospheric concentrations of grass pollen. A method based on meteorological factors and grain crop estimates. Clin Exp Allergy. 1992 May;22(5):540-6.
4) Subiza J, Jerez M, Jiménez JA, Narganes MJ, Cabrera M, Varela S, Subiza E. Allergenic pollen pollinosis in Madrid. J Allergy Clin Immunol. 1995 Jul;96(1):15-23.
5) Varela S, Subiza J, Subiza JL, Rodríguez R, García B, Jerez M, Jiménez JA, Panzani R. Platanus pollen as an important cause of pollinosis. J Allergy Clin Immunol. 1997 Dec;100(6 Pt 1):748-54. 6) Cabrera M, Subiza J, Fernández-Caldas E, Garzón García B, Moreno-Grau S, Subiza JL. Influence of environmental drivers on allergy to pollen grains in a case study in Spain (Madrid): meteorological factors, pollutants, and airborne concentration of aeroallergens. Environ Sci Pollut Res Int. 2021 Oct;28(38):53614-53628.
7) Pedrosa M, Guerrero-Sanchez VM, Canales-Bueno N, Loli-Ausejo D, Castillejo MÁ, Quirce S, Jorrin-Novo JV, Rodriguez-Perez R. Quercus ilex pollen allergen, Que i 1, responsible for pollen food allergy syndrome caused by fruits in Spanish allergic patients. Clin Exp Allergy. 2020 Jul;50(7):815-823.
8) Subiza J, Cabrera M, Jm CR, Jc C, Mj N. Influence of climate change on airborne pollen concentrations in Madrid, 1979-2018. Clin Exp Allergy. 2022 Apr;52(4):574-577.